
Strukturierte Brustimplantate aufgrund von Krebsverbindung zurückgerufen

Allergan Inc. Letzte Woche wurden laut einer Pressemitteilung freiwillig mehrere Modelle texturierter Brustimplantate zurückgerufen, nachdem Bedenken laut wurden, dass sie mit einer seltenen Form von Krebs in Verbindung gebracht werden könnten, einem mit Brustimplantaten assoziierten anaplastischen großzelligen Lymphom. Die Food and Drug Administration hatte das Unternehmen aufgefordert, einige seiner Implantate und Gewebeexpander vom Markt zu nehmen, nachdem neue Informationen eine unverhältnismäßig große Anzahl von BIA-ALCL-Fällen bei Menschen mit den Produkten enthüllten.
BIA-ALCL, eine Art von Non-Hodgkin-Lymphom, wurde stark mit strukturierten Implantaten in Verbindung gebracht, die weniger als 5 Prozent der in den USA verkauften Implantate ausmachen.S., nach Angaben der FDA. Die meisten in den USA verkauften Implantate haben glatte Oberflächen, aber die Biocell-Implantate von Allergan verfügen über eine makrotexturierte Oberfläche, die für das Unternehmen einzigartig ist.
„Obwohl die Gesamtinzidenz von BIA-ALCL relativ gering zu sein scheint, hat die FDA Maßnahmen ergriffen, um das Unternehmen auf neue Beweise aufmerksam zu machen, die auf a hinweisen Rückruf ist gerechtfertigt, um die Gesundheit von Frauen zu schützen “, sagte Amy Abernethy, stellvertretende Hauptkommissarin der FDA, M.D., Ph.D., sagte in einer Erklärung. Sie fügte hinzu, dass die FDA seit 2011 den Zusammenhang zwischen Brustimplantaten und BIA-ALCL überwacht.
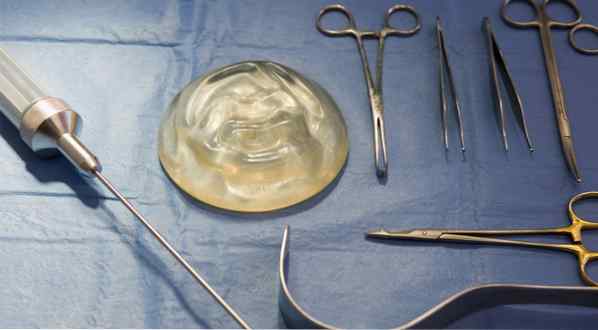
Alles, was Sie über Brustimplantate wissen müssen
Machen Sie Ihre Recherchen, bevor Sie diese gewaltige Verpflichtung eingehen.
Artikel lesenDie FDA beantragte den Rückruf, nachdem eine aktualisierte Analyse ergab, dass von 573 Personen mit BIA-ALCL weltweit 481 Berichten zufolge Allergan-Brustimplantate hatten. In Anbetracht der neuen Daten besagt die Analyse der FDA, dass das Risiko von BIA-ALCL bei Patienten mit Allergan Biocell-Implantaten sechsmal höher ist als bei Patienten mit strukturierten Implantaten anderer Hersteller. BIA-ALCL befindet sich normalerweise im Narbengewebe und in der Flüssigkeit in der Nähe eines Implantats.
Die Nachricht mag für jeden, der bereits über die jetzt zurückgerufenen Implantate verfügt, beunruhigend sein, aber die FDA fordert nicht, dass sie bei symptomlosen Patienten entfernt werden. Die Ankündigung des Rückrufs soll lediglich Patienten und Ärzte auf den Zusammenhang aufmerksam machen.
"Wir werden ständig neue Informationen auswerten und können daher Maßnahmen in Bezug auf andere Brustimplantate ergreifen, wenn dies gerechtfertigt ist", so Jeff Shuren, M.D., J.D., sagte der Direktor des FDA-Zentrums für Geräte und radiologische Gesundheit. „Darüber hinaus setzen wir unsere Bewertung fort, um festzustellen, ob das Risiko für die Entwicklung von BIA-ALCL auf bestimmte Modelle strukturierter oder aller strukturierten Brustimplantate beschränkt ist. Wir weisen Frauen und Angehörige der Gesundheitsberufe weiterhin darauf hin, dass die Verwendung von Brustimplantaten mit einem Risiko für die Entwicklung von BIA-ALCL verbunden ist und dass das Risiko bei strukturierten Implantaten höher ist.”
Auch hier rät die FDA Personen ohne Symptome nicht, die zurückgerufenen Implantate entfernen zu lassen, bietet jedoch eine Liste mit wichtigen Informationen und Empfehlungen für Personen mit Aufzählungszeichen. Holen Sie sich die vollständige Liste am Ende von die Pressemitteilung der FDA.Regierung, und informieren Sie Ihren Arzt, wenn Sie Bedenken bezüglich Implantaten haben.

Frauen nutzen soziale Medien, um ihre…
Immer mehr Frauen teilen ihre Geschichten in sozialen Medien.
Artikel lesen


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.